変分原理と変化の向き
変分原理
「変分原理」とは「何か基本的な量の変化を考えることで法則を導く原理」ということで、多くの場合ある量の変化量が0になるところを求めるとそれが求めたい状態であるという形で使う。
変分原理は解析力学でも「作用が停留するのが実現する運動である」という形で使った。あるいは静力学でも「エネルギー最低の位置が安定点である」という考え方で使う。
静力学の場合
解析力学までいくと説明することが多くなるので、静力学の場合で考えよう。無重力状態でバネ定数$k$のバネにつながれた物体を考えると、弾性力の位置エネルギー${1\over 2}kx^2$($x$は自然長からの伸び)だから、これが最小になるのは$x=0$の点(自然長のとき)である。
ここに重力があるとすると、重力の位置エネルギー$mgx$が加わる($x$が上向き、つまり$x$が増加すると位置エネルギーが増える方向の座標だったとしよう)。このときは全位置エネルギーは$U={1\over2}kx^2+mgx$だから、これが最小になるのは${\mathrm dU\over\mathrm dx}=kx+mg$が0になるところだから、$x=-{mg\over k}$のところである。
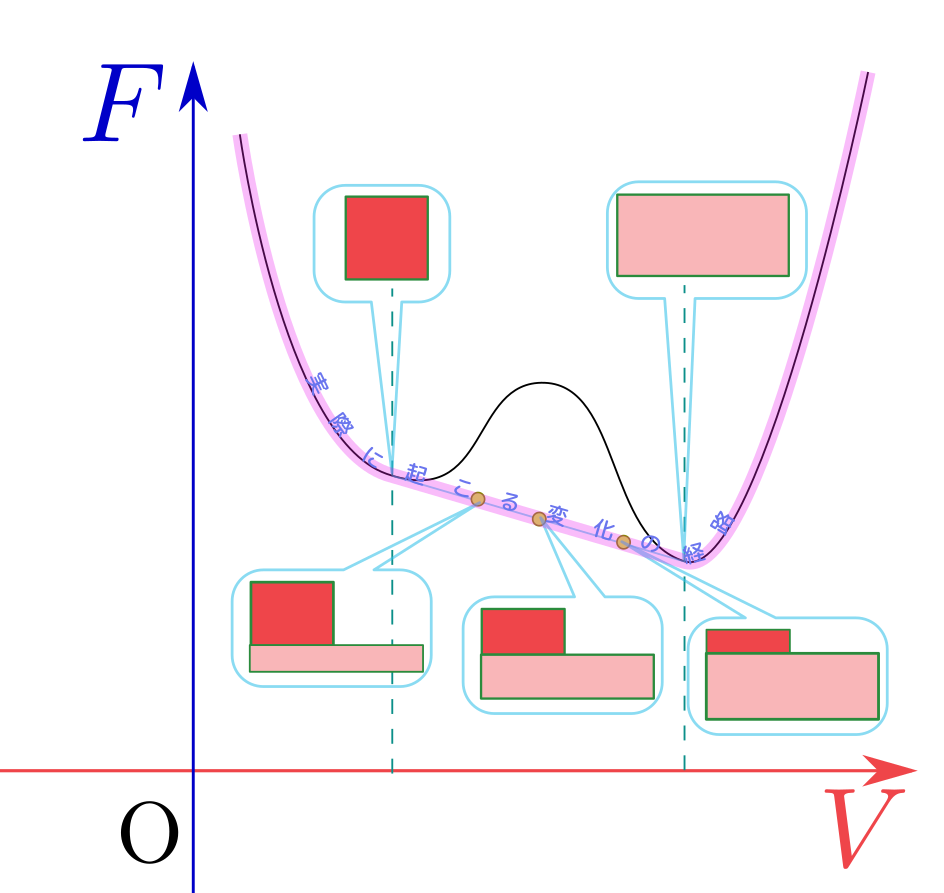
もし今位置エネルギー最小の点($x=-{mg\over k}$)じゃない場所に物体がいたとしたら、その場所へ向かう方向に力が働き、(摩擦などによるエネルギーの散逸を得て)位置エネルギー最小点に落ち着くだろう。
熱力学でも$U$や$F$などのエネルギーを最小化する方向へ変化が起こるという考え方で物理現象を予言しよう、というのが変分原理である。
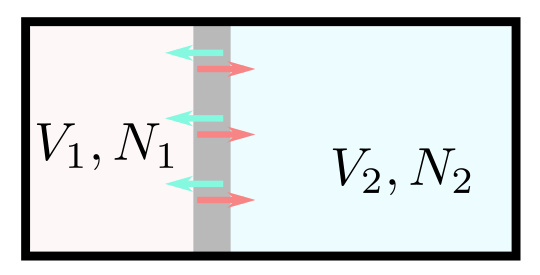
平衡状態にある二つの系$(T;V_1,N_1)$と$(T;V_2,N_2)$を接触させて壁を取り除いてしばらく待つと、$(T,\underbrace{V_1+V_2}_V,\underbrace{N_1+N_2}_N)$という平衡状態に達する(温度は最初から同じであったことに注意)。
このとき、ヘルムホルツの自由エネルギーの差
$$ F[T;V_1,N_1]+F[T;V_2,N_2]-F[T;V,N] $$を考えると、これはこの変化を行った時の最大仕事である。しかし最大仕事が行われるのは準静的な操作の時で、単に壁を取り除くという操作は準静的ではないからその時の仕事は最大仕事ではない。壁を取り除いただけでは何も動かしたりしないから、仕事は0である。最大仕事は0よりは大きいことだけはわかるから、
$$ F[T;V_1,N_1]+F[T;V_2,N_2]-F[T;V,N]\geq 0 $$という不等式を満たす。つまり
$$ F[T;V_1,N_1]+F[T;V_2,N_2]\geq F[T;V,N] $$で、「壁を取り払って(たとえば)気体を混ぜてしまうと、ヘルムホルツ自由エネルギーは減る(か変化しない)」ということがわかる。
二つの系が物質量$N$のやりとりができる状況にしてみよう(具体的には、壁に穴を開けて空気分子などが行き来できるようにする)。すると、最初$N_1,N_2$だった物質量が、$\tilde N_1,\tilde N_2$(もちろん、$N_1+N_2=\tilde N_1+\tilde N_2=N$)になったところで平衡に達したとしよう。この時もヘルムホルツ自由エネルギーは減る(か、変化しない)はずで、逆に言えば「もう減らせない」というところで変化が止まるはず、と考えると、
$$ F[T;V_1,\tilde N_1]+F[T;V_2,\tilde N_2]=\min_{N_1,N_2\atop N_1+N_2=N}F[T;V_1,N_1]+F[T;V_2,N_2] $$が成立するだろう(最小値が一個じゃない場合については後で考える)。
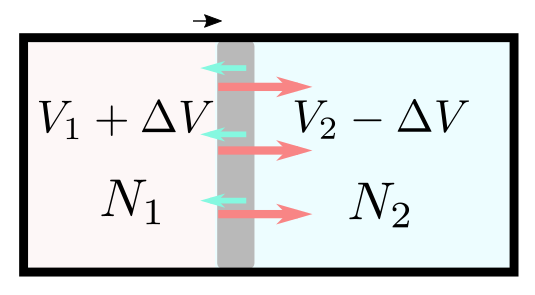
体積がやりとりされる(間の壁が押されて動くような状況)についても同様に、
$$ F[T;\tilde V_1,N_1]+F[T;\tilde V_2,N_2]=\min_{V_1,V_2\atop V_1+V_2=V}F[T;V_1,N_1]+F[T;V_2,N_2] $$が成立する。
理想気体の場合、$F=-NRT\log V+(Vに依らない部分)$だから、 $$ F[T;V_1,N_1]+F[T;V_2,N_2]=-N_1 RT \log V_1 -N_2 RT \log V_2 + (V_1,V_2に依らない部分) $$ という式で書ける。
$V_2=V-V_1$としてグラフを描くと

となって、どこかに最小値が確かにある(具体的計算とその意味は後で)。

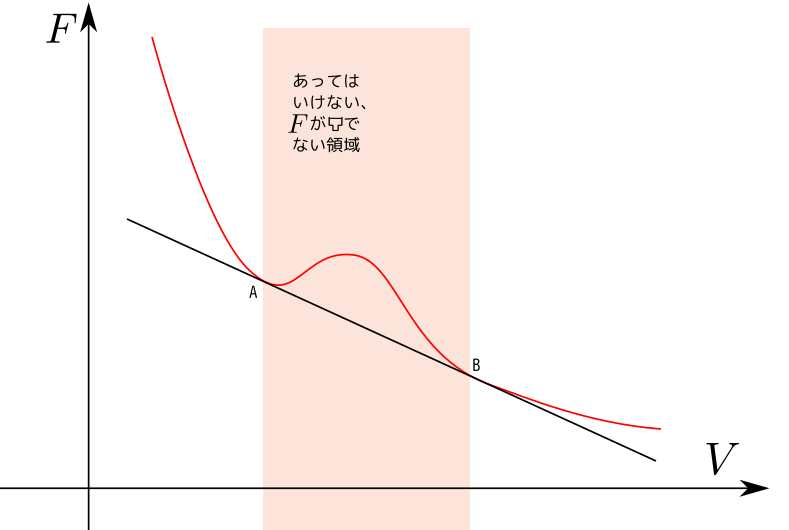
 )」でなかったらどういうおかしいことが起こるかを一つの例で示そう。
)」でなかったらどういうおかしいことが起こるかを一つの例で示そう。