熱力学2015年度第3回
では準静的操作と最大仕事というキーワードについて、アニメーションなどを見ながら説明した。
平衡状態
熱力学が考える理想的状況をピストンの場合で説明すると、

のように、ピストンを引いた直後の「左が高温・高圧で右が低温・低圧」という状況は「平衡状態」ではない。
しばらく待つと、

のように全体の温度・圧力(密度も)が一様になり、「平衡状態」に達する。
というわけで、ざっくり言えば「じゅうぶんゆっくり(つまり準静的に)変化するのであれば、途中の状態もすべて平衡状態を保ったまま変化していくと考えてよい」ということになる。
平衡状態は温度・圧力などが一様なので、「温度は$T$です」「圧力は$P$です」と語ることで状態を指定できるが、平衡でない状態では「左の方の温度は$T_1$で、右に行くほどだんだん低くなって最後は$T_2$に」というふうに、場所の関数である温度変数$T(x)$を使わないと状態が指定できない。つまり、平衡状態の方が使う変数が少なくて済む。
こう言うと、楽だからとズルをしているように思えるかもしれない。しかし大事なことは、「考える状態を平衡状態に限る」という(「ズル」に見えかねない)簡単化をしてもなお、熱力学という学問はとても役に立つということだ。たとえば力学における「摩擦がないとする」というのも「ズル」っぽいと言えば「ズル」なのだが、摩擦がないという簡単化をしてなお、力学は豊富な内容と実用性を持っている。
示量変数
気体の状態を指定する変数としては温度$T$、圧力$P$、体積$V$、物質量Nなどが思い浮かぶ。このうち体積$V$と物質量(モル数)Nは相加的(additive)であるという性質を持っている(たとえば体積$V'$の系と体積$V''$の系を合わせると$V'+V''$の系になる)。
状態を指定する変数の中で、
を「示量変数」(extensive varijable)と呼ぶ(漢字の方が意味がわかりやすい)。
気体の場合、体積$V$と物質量(モル数)$N$が示量変数である。
この後「示量変数を変化させる」という操作を行うのだけど、たとえば体積変化を起こすとその手応えは圧力として出現する。
系全体を大きくしても変化しない変数は「示強変数」(intensive variable)である。圧力$P$や温度$T$はこちらに属する(100度の水と100度の水を合わせたら200度になったらびっくりする)。
熱力学の視点
熱力学は、「実際には$6\times10^{23}$程度の自由度がある系」をまじめに考えるという方向の学問ではなく、むしろ、「外部からする操作の種類」程度の数の変数だけで系を代表させて考えていく。
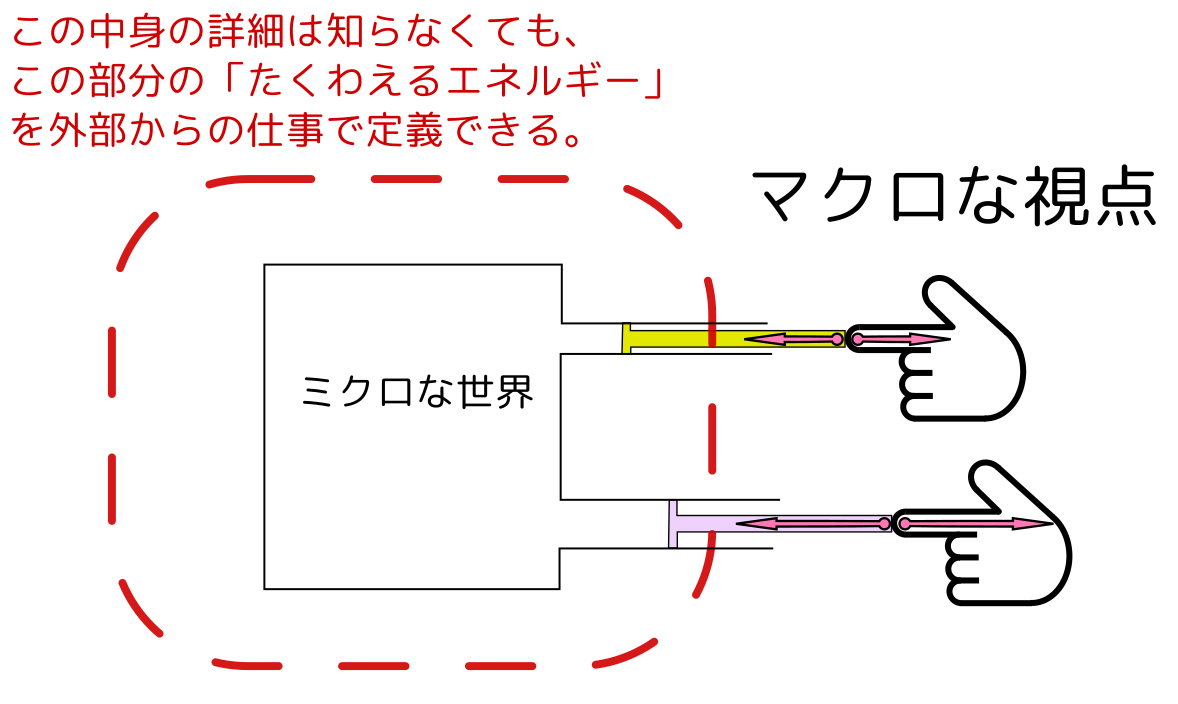
上の図の場合、操作できるのが二つのピストンがあり、それぞれを押したり引いたりするとどの程度仕事がされるか、ということは「手」の動きと「手応え」で計算できる。それに応じて系のエネルギーに対応するものが増えたり減ったりする(前に説明したようにこの時の仕事は変化のさせ方によって違うからエネルギーをちゃんと定義するには「準静的に」とか「最大仕事になるように」とか変化方法を指定する必要がある)。
等温環境での平衡状態
実際に実験を行う時の状況として「実験装置(系)を周囲の温度と同じにする」という状況がある。この時(例によって準静的に変化が起こるとすれば)、系の温度は一定である(実際には変化の最初と最後以外では温度が変わっている可能性はある)。
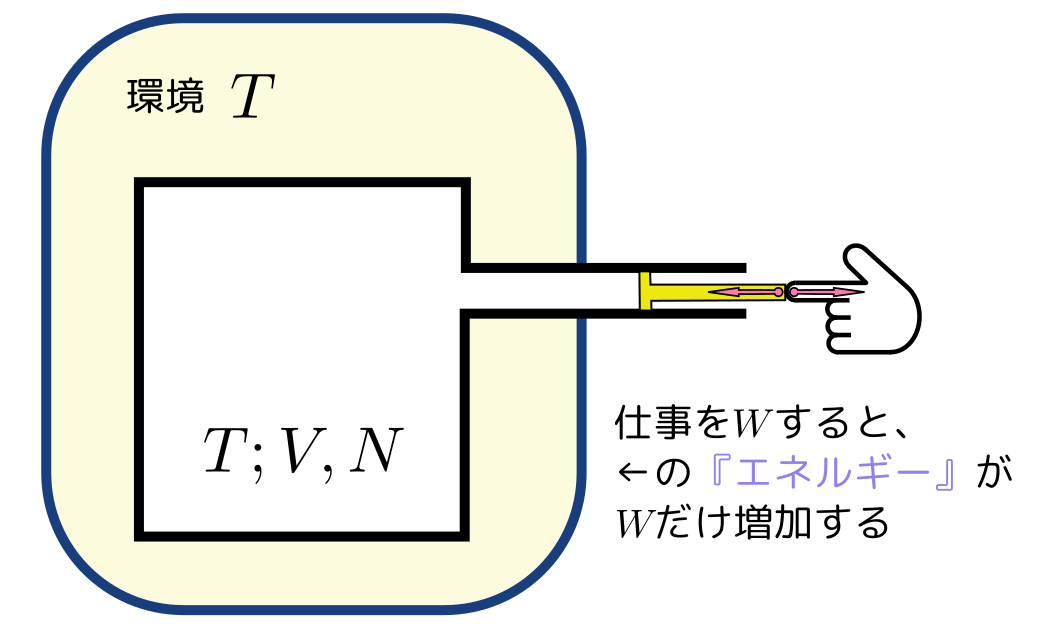
このような系の状態を記述するには、まず「外部から操作できる示量変数」である$X$($V,N$をまとめてこう書く)と、「外部環境が決める示強変数」である$T$が必要である。つまり、$(T;X)$(;で分けたのは(示強;示量)ということ)変数で系の平衡状態が定義できる(くどいようだがもう一度、こんなふうに少数の変数で系の状態が指定できてしまうのは、平衡状態だからである)。
こういう系が等温に保たれる状態で系に仕事をさせると、その分系の『エネルギー』括弧つきで書いたのは、普通のエネルギーとはちょっと違うからである。が変化する。
断熱された系の平衡状態
次に、周りとの接触を断って、「熱」(がまだ何なのかは説明していないが)が出入りしないという「断熱された系」を考える。今度は周りとの影響を遮断されているわけだから(たとえば魔法瓶では壁の中に真空を使うことでそれに似た状況を作っている)。
この時の仕事によって変化する量として、さっきのヘルムホルツの自由エネルギーとは別の『エネルギー』を定義することができる。
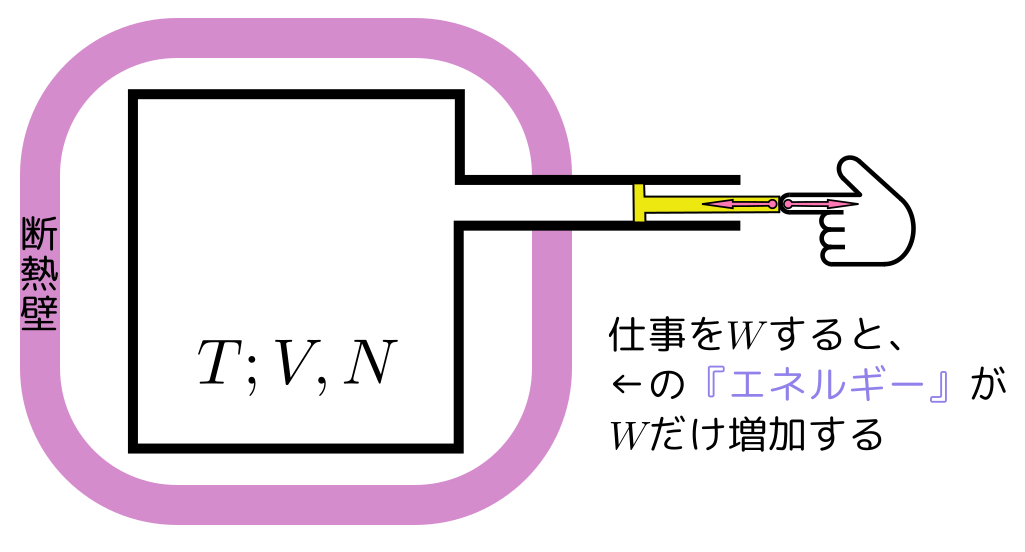
こっちは内部エネルギー$U$と呼ばれる。環境と相互作用がないから、内部エネルギーは系が持っていると考えて良い(力学でのエネルギーに近いのはこっちだろう)。
この場合外界との影響は断っているので、内部の温度$T$は環境の温度とは関係ない量である(そして、実際のところ体積を変化させると連動して変化する)。
今回使っている教科書では「熱」というよくわからない、目に見えないものは後で定義することにして、上で述べたような「操作とそれに対する手応え」で計算できるところの(つまり「目に見えるものから計算できる量」であるところの)「ヘルムホルツの自由エネルギー」や「内部エネルギー」を先に定義していく。
こうして等温操作と断熱操作を比較してみると、等温操作の時には$T$が「環境の温度」であって環境を決めれば決まる変数だったのにたいし、断熱操作では(ピストンを動かすという)操作によって$V$と連動して変化する変数になっているという違いが見て取れる。よって等温操作では$V$と独立な変数である$T$は、断熱操作においてはそうならない。